
Vaccine chống Covid-19
Khi loài coronavirus vừa mới khởi phát ra dịch cúm ở Vũ Hán, tôi nghe các bác sỹ của Bệnh viện Nhiệt đới TPHCM gọi tắt nó một cách dân dã là Cô Vi. Sau này, WHO đặt ra những cái tên dài dòng như SARS-CoV-2, rồi Covid-19. Trong bài này, tôi xin phép dùng lại từ Cô Vi để chỉ tên con virus nguy hiểm này.
Biện pháp căn cơ nhất để khắc phục những đại dịch như Cô Vi là tạo ra miễn dịch cộng đồng bằng cách tiêm chủng (vaccine).
Chúng ta biết điểm yếu quan trọng nhất của virus là nó không tự nhân bản được bên ngoài cơ thể. Một khi đa số cư dân đã được tiêm chủng thì virus có thể tự diệt vong do không tìm được vật chủ để lan truyền tiếp.
Khi kẻ cướp thành chủ nhà
Quan hệ giữa virus với tế bào có thể ví như giữa kẻ cướp với chủ nhà.
Chủ nhà - tế bào là đơn vị cấu trúc-chức năng cơ bản của cơ thể. Hai thành phần chính của tế bào có chứa thông tin di truyền trong cấu trúc phân tử là DNA/RNA và protein.
Protein tạo ra các cấu trúc và điều khiển thực hiện hầu hết các quá trình hoạt động tế bào. DNA như tập sách chứa thông tin di truyền để phiên dịch ra mọi loại protein.
DNA được bảo vệ kỹ lưỡng trong nhân tế bào, từ DNA mới sao chép ra các đoạn RNA nhỏ hơn, trong đó có các đoạn mRNA được chuyển ra ngoài bào tương. Thông tin di truyền từ mRNA được chuyển tới các hạt (gọi là ribosome), rồi được phiên dịch thành ra cấu trúc protein.
Thông tin di truyền khi đã phiên dịch sang protein thì không thể phiên dịch ngược lại mRNA hay DNA được nữa.
Kẻ cướp – virus là những hạt cực nhỏ, chỉ gồm có vật liệu chứa thông tin di truyền (DNA/RNA) và lớp vỏ protein tối thiểu. Khi xâm nhập vào tế bào, DNA/RNA của virus cướp lấy bộ máy protein của tế bào, điều khiển tế bào tổng hợp ra thật nhiều DNA/RNA/protein của virus, lắp ráp thành ra các hạt virus mới.
Tế bào không chịu nổi mà vỡ ra, giải phóng ra các hạt virus, chúng tiếp tục đi tìm và đột nhập vào các tế bào khác.
Có hai loại virus là DNA và RNA. Virus DNA dùng DNA làm vật liệu chứa thông tin di truyền. Sau khi lọt vào tế bào, DNA của virus sai khiến các cỗ máy protein của tế bào tổng hợp ra mRNA và protein của nó. DNA virus có thể được tích hợp vào DNA của tế bào, tạo ra dạng nhiễm tiềm ẩn.
Virus RNA tối giản hơn nữa, chỉ cần RNA và lớp vỏ protein là đủ để xuất khẩu khỏi tế bào, gây nhiễm các tế bào khác.
Cô Vi thuộc loại virus RNA chuỗi đơn. RNA chuỗi đơn kém bền vững hơn DNA, do đó khả năng biến dị của virus RNA mạnh hơn, rất nhanh chóng tạo ra các biến thể mới.
Virus không phải là những tế bào sống, không thể tự nhân bản bên ngoài tế bào. Tuy chỉ ký sinh trong vật chủ, virus vẫn tiến hóa song hành với vật chủ. Lớp vỏ protein của virus thường chứa những phân tử cấu trúc bắt chước các phân tử miễn dịch của tế bào, làm cho tế bào tiếp nhận nhầm vào bên trong.
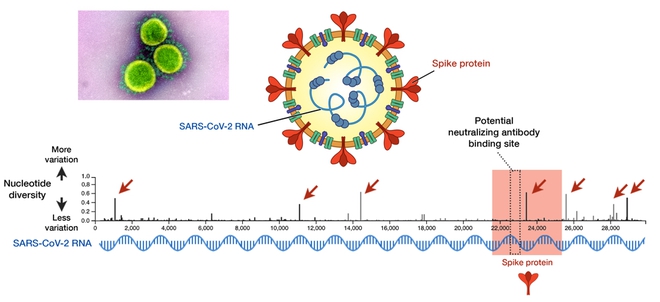
Trong trường hợp Cô Vi, protein S (S viết tắt từ "spike" = cái gai) trên vỏ của nó có cấu trúc bắt chước phân tử ACE (angiotensin-converting enzyme) của tế bào.
Mục tiêu của vaccine
Mục tiêu của vaccine là làm cho hệ thống miễn dịch nhận biết được và "khóa tay" kẻ cướp-virus trước khi nó xâm nhập được vào tế bào. Protein S là mục tiêu then chốt khi thiết kế vaccine chống Cô Vi.
Protein S được "giới thiệu" cho các tế bào miễn dịch nhận mặt theo nhiều cách khác nhau tùy theo loại vaccine, nhưng tất cả đều nhằm kích thích sản xuất ra các kháng thể trung hòa protein S.
Các kháng thể này lưu thông trong máu, khi có virus xâm nhập thì kháng thể bao bọc ngay lên các gai protein S, khiến cho virus không còn chỗ để dính bám vào bề mặt tế bào nữa. Khi không lọt được vào tế bào thì virus không có cách gì nhân bản được, chỉ còn chờ bị tiêu hủy.
Có thể đưa protein S vào cơ thể qua việc tiêm các hạt virus bất hoạt (không còn khả năng nhân bản). Nhưng protein S kém bền vững nên mau chóng bị phân hủy, hiệu quả kích thích miễn dịch kém.
Trong công nghệ mới nhất, vaccine DNA/RNA, người ta đưa vào tế bào đoạn DNA/RNA mã hóa thông tin tổng hợp ra protein S, bằng cách đó tạo ra hiệu quả kích thích miễn dịch cao hơn.

Vaccine RNA
Tại Australia và nhiều nước phát triển khác, các loại vaccine với Cô Vi được chấp nhận phổ biến là Pfizer (RNA) và AstraZeneca (DNA), đều không đưa hạt coronavirus hay protein S vào cơ thể.
Vaccine RNA là công nghệ rất mới, chỉ mới được chính thức áp dụng cho người hồi tháng 12 năm ngoái. Hiện có vaccine Pfizer (hợp tác giữa BioNTech của Đức với Pfizer của Mỹ) và vaccine Moderna (Mỹ) áp dụng công nghệ này.
Người ta bao đoạn mRNA mã hóa protein S vào trong những nang lipid cực nhỏ. Khi được tiêm vào cơ thể thì những nang này được tế bào nuốt vào, mRNA điều khiển tế bào tổng hợp ra protein S mà không tạo ra hạt virus.
Ưu điểm của vaccine RNA cho đến nay như được biết thông qua các chiến dịch tiêm chủng tại Mỹ và châu Âu là khá an toàn, đạt được hiệu quả bảo vệ cao.
Nhược điểm của nó là đắt tiền, và vì cấu trúc RNA không bền vững nên vaccine phải được bảo quản trong tủ lạnh sâu (âm 80oC), khó vận chuyển. Một nhược điểm nữa là nếu phải tiêm nhiều lần thì vaccine RNA có thể gây hiệu ứng phụ mạnh hơn.
Vaccine DNA
Các vaccine AstraZeneca (Oxford, UK), J&J (Johnson & Johnson), Sputnik-V (Viện Gamalea, CHLB Nga) dùng đoạn DNA được sao chép ngược từ đoạn RNA chứa thông tin tổng hợp protein S của Cô Vi.
Để đưa đoạn DNA này vào tế bào, phải dùng một loại virus lành tính với người làm vector chuyên chở. Vaccine AstraZeneca dùng adenovirus của vượn, còn vaccine Sputnik-V dùng adenovirus của người làm vector.
Vì nước Nga quá rộng, vaccine Sputnik-V được bào chế thành 2 loại, loại lỏng chỉ cần cất giữ trong ngăn đá của tủ lạnh thường, và loại bột có thể để ở nhiệt độ thường, trước khi dùng thì mới hòa nước cất. DNA khá bền vững nên ngay cả khi ở dạng lỏng cũng chỉ cần bảo quản ở tủ lạnh thường.
Vaccine DNA cũng đạt hiệu quả bảo vệ tương đối cao. Tuy nhiên qua việc thử trên diện rộng, người ta phát hiện ra vaccine này có thể gây ra hiện tượng đông máu tuy rất hiếm nhưng có thể gây tử vong.
Một nhược điểm nữa của vaccine DNA có thể chưa được đánh giá chi tiết, là các adenovirus lành tính được sử dụng làm vector khi được tiêm nhiều lần vào cơ thể thì có thể tạo ra đáp ứng miễn dịch để bị tiêu hủy.

Vaccine toàn hạt
Công nghệ vaccine dùng DNA/RNA rất mới và khá đắt tiền, khó phổ cập cho các nước nghèo. Vì thế nhiều nước khác vẫn phải sử dụng loại vaccine toàn hạt coronavirus theo công nghệ truyền thống.
Ví dụ như trường hợp vaccine Sinovac (CoronaVac, China), Cô Vi được phân lập từ người bệnh rồi nhân bản thành lượng lớn trong phòng thí nghiệm. Virus được làm bất hoạt, làm phân hủy RNA, virus không còn khả năng nhân bản tiếp. Khi tiêm vào cơ thể người, protein S vẫn còn tương đối nguyên vẹn nên sẽ kích hoạt được các tế bào miễn dịch.
Như đã nêu trên, protein S của coronavirus kém bền, mau phân hủy. Có lẽ đó là nguyên nhân khiến cho hiệu quả của Sinovac khá thất thường. Mặc dù thông báo từ China đưa chỉ số bảo vệ khỏi triệu chứng nhiễm Cô Vi cao hơn, nhưng sau những chiến dịch tiêm chủng lớn, tại Chile con số này là 67%, tại Brazil là 50.4%.
Vaccine NDV-HXP-S. Ba cơ quan uy tín tại Mỹ là "University of Texas at Austin", "Icahn School of Medicine at Mount Sinai", và "National Institute of Allergy and Infectious Diseases Vaccine Research Center" đã hợp tác nghiên cứu nhằm tạo ra công nghệ vaccine phổ cập cho các nước nghèo, dựa trên công nghệ truyền thống nuôi cấy virus trên phôi gà vốn đã có từ những năm 1950s.
Điểm khác biệt trung tâm ở vaccine NVD-HXP-S là họ đã nghiên cứu ra phân tử protein S "nhân tạo" chứa 6 axit amin proline, phân tử này bền vững hơn hẳn protein S bình thường chỉ có 2 proline, nhờ vậy có hoạt tính kích thích miễn dịch cao hơn.
Các nhà khoa học Mỹ tuyên bố sẽ chuyển giao công nghệ này miễn phí cho tất cả các nước nào mong muốn. Brazil, Mehico, Thái Lan và Việt Nam là những nước đầu tiên đã ký được thỏa thuận tiếp nhận công nghệ này
Viện Vaccine và Sinh phẩm Y tế Việt Nam đã tiếp nhận công nghệ vaccine NDV-HXP-6 này và đặt tên là COVIVAC
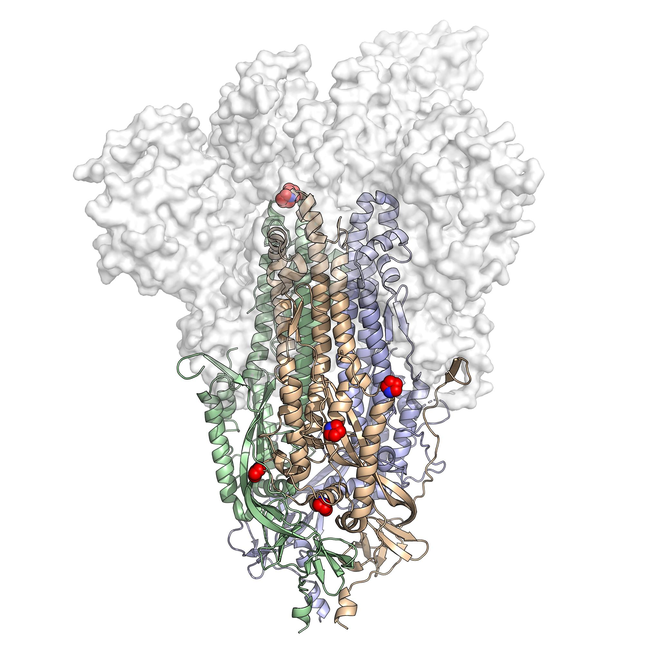
Hình minh họa: Mô hình phân tử protein S nhân tạo có 6 gốc Proline (màu đỏ). Photocourtesy University of Texas at Austin.
Phối hợp vaccine
Thường thì để đạt hiệu quả cao, đa số các vaccine thường dùng 2 mũi, mũi đầu (prime) để "giới thiệu" cho các tế bào miễn dịch biết "mặt mũi" con vi khuẩn/virus gây bệnh thế nào. Trong cơ thể người được tiêm sẽ sản xuất ra kháng thể, nhưng chưa thật nhiều.
Sau thời gian vài tuần, mũi vaccine thứ hai (boost) được tiếp tục để tăng cường miễn dịch. Các tế bào miễn dịch đã nhớ được mầm bệnh từ mũi thứ nhất này nhanh chóng phân chia, tạo ra số lượng lớn tế bào và kháng thể, có tác dụng trung hòa ngay mầm bệnh khi chúng vừa xâm nhập cơ thể.
Về mặt miễn dịch học, mũi vaccine thứ nhất (giới thiệu) và thứ hai (tăng cường) không nhất thiết phải cùng một chủng loại. Chiến lược phối hợp các loại vaccine từ các nhà sản xuất khác nhau đã được áp dụng có kết quả trước đây trong dịch Ebola, nay đang được các nhà miễn dịch học nghiên cứu áp dụng cho Cô Vi.
Tại Anh Quốc, khoảng 1000 người tình nguyện đã được lựa chọn cho việc thử nghiệm 8 cách kết hợp của 4 loại vaccine khác nhau (Pfizer, AstraZeneca, Moderna và Novavax).
Một nghiên cứu khác cũng vừa được tờ Nature đưa tin kết quả sơ bộ tại Tây Ban Nha, trong hơn 600 người tình nguyện đã được tiêm vaccine AstraZeneca thì 2/3 được tăng cường bằng vaccine Pfizer.
Kết quả sơ bộ cho thấy việc phối hợp vaccine khác loại vẫn tạo ra tăng cường miễn dịch, đôi khi có thể vượt trội so với khi dùng vaccine cùng loại. Có vẻ như phối hợp vaccine cũng gây ra tỷ lệ phản ứng phụ, nhưng đều là những phản ứng nhẹ.
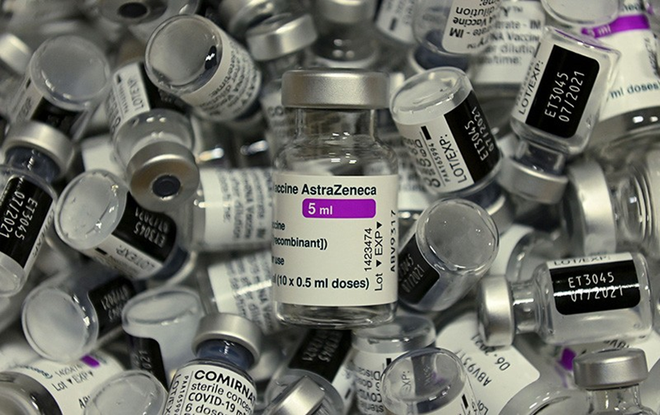
Hình minh họa: Trộn vaccine. Credit: Christof Stache/AFP/Getty.
Nghiên cứu phối hợp vaccine nếu thành công sẽ mang lại nhiều lợi ích.
Chiến lược chung của các quốc gia là nhanh chóng phủ được càng rộng càng tốt tỷ lệ dân cư được tiêm ít nhất một mũi vaccine. Như vậy sẽ có rất nhiều người phải chờ nhiều tuần hay nhiều tháng mới nhận được vaccine tăng cường.
Với nhiều quốc gia nghèo không tự chủ được công nghệ vaccine, thì nguồn vaccine có thể phải thay đổi, người đã tiêm loại một vaccine này chưa chắc đã có được đúng chủng loại vaccine đó để tiêm mũi tăng cường. Việc kết hợp được các nguồn vaccine khác nhau sẽ góp phần giải quyết được khó khăn lớn này.
Đầu tháng trước tại Thành Đô, Trung Quốc, sau khi vaccine Sinovac bị đánh giá là hiệu quả không cao, ông Gao Fu, giám đốc Cơ quan Kiểm soát Bệnh China (CDC) đã tuyên bố có thể nghiên cứu phối hợp với một loại vaccine RNA.
Đối với các nước châu Âu do có lo ngại về phản ứng đông máu ở phụ nữ trẻ nên có nhiều người đã tiêm mũi đầu là vaccine AstraZeneca rồi, thì nay có thể xem xét được tăng cường bằng vaccine Pfizer chẳng hạn.
Chưa kể đến là chúng ta còn chưa biết được trong tương lai nếu bị Cô Vi quay trở lại thăm với các biến chủng mới, có bắt buộc phải tiêm thêm vaccine "nhắc nhở" (mũi thứ ba hay nhiều hơn nữa) hay không.
Việc tiêm nhắc lại nhiều lần cùng một loại vaccine có thể kèm theo những hệ lụy; như vaccine DNA thì trở nên kém tác dụng do cơ thể phát sinh đáp ứng miễn dịch chống lại adenovirus, còn vaccine RNA thì gây ra phản ứng phụ mạnh hơn.




